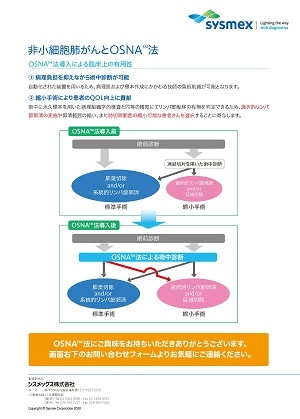
OSNA™ (One-Step Nucleic Acid Amplification)法は核酸の抽出・精製が不要でワンステップでの増幅を可能する技術です。この技術を利用し、専用の遺伝子増幅検出装置・試薬を用いて、可溶化したリンパ節中に含まれる標的遺伝子サイトケラチン19mRNAを増幅・検出することで、リンパ節へのがん転移の判定の補助を行います。
リンパ節中の標的遺伝子を高精度、迅速、簡便に検出することが可能となります。また、乳がん、大腸がん、胃がん、非小細胞肺がんに対して保険適用されています。
がんリンパ節転移診断システム(OSNA™法) 遺伝子増幅検出装置 RD-200
シスメックスアイランドとは、シスメックスのバーチャル空間サイトです。
展示会にいるような3D空間で、製品について深く知ることができます。
OSNA™ (One-Step Nucleic Acid Amplification)法は核酸の抽出・精製が不要でワンステップでの増幅を可能する技術です。この技術を利用し、専用の遺伝子増幅検出装置・試薬を用いて、可溶化したリンパ節中に含まれる標的遺伝子サイトケラチン19mRNAを増幅・検出することで、リンパ節へのがん転移の判定の補助を行います。
リンパ節中の標的遺伝子を高精度、迅速、簡便に検出することが可能となります。また、乳がん、大腸がん、胃がん、非小細胞肺がんに対して保険適用されています。
医療機器製造販売届出番号
RD-200:28B1X10014000040
RD-100i:28B1X10014000032
OSNA™とは?
- サイトケラチン19(CK19)mRNAを増幅検出し癌リンパ節転移診断をサポート
- 保険適応2,400点:乳癌、大腸癌、胃癌、非小細胞肺癌
- OSNA™法によるメリット
- 1簡易にリンパ節転移検査を実施可能
- 2精度高い検査結果の取得
- 3迅速な検査時間
- 4リンパ節転移診断の標準化に貢献
- 5病理医の労力削減
- 6豊富な採用実績
- 7安心のオンラインサポート
測定フロー

保険償還価格
| 区分番号 | 測定項目 | 測定方法 | 保険点数 |
|---|---|---|---|
| D006-8 | サイトケラチン19 (KRT19)mRNA検出 |
OSNA(One-Step Nucleic Acid Amplification)法 |
2400点 |
留意事項
サイトケラチン19(KRT19)mRNA検出は、視触診等による診断または術前の画像診断でリンパ節転移陽性が明らかでない乳癌、胃癌、大腸癌又は非小細胞肺癌患者に対して、摘出された乳癌、胃癌、大腸癌又は非小細胞肺癌所属リンパ節中のサイトケラチン19(KRT19)mRNAの検出によるリンパ節転移診断及び術式の選択等の治療方針の決定の補助を目的としてOSNA(One-Step Nucleic Acid Amplification)法により測定を行った場合に、一連につき1回に限り算定する。
「OSNA™」と「現行法」の違い
現行法による検査の場合
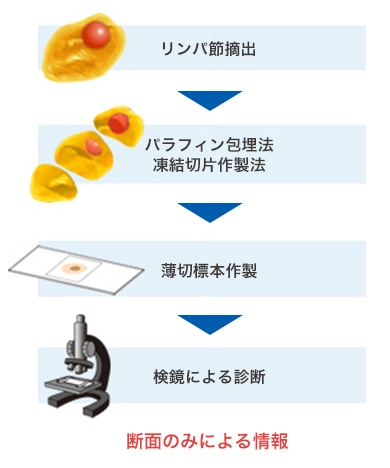
【病理組織調査】
手術中に病理医が
顕微鏡でがん細胞の有無を確認
病理組織学的アプローチであるこれまでの方法では、専門病理医の技術や経験に頼るところが大きく、限られた時間での検査には施設間差があるといわれています。
課題とされる点:
- リンパ節の一部のみの検査のため、がん転移を見つけられない場合がある
- 手術中という限られた時間でのきめ細かな観察が必要
- 正確な判定には、専門病理医の技術と経験が必要
OSNA™法による検査の場合
現行法による検査の場合
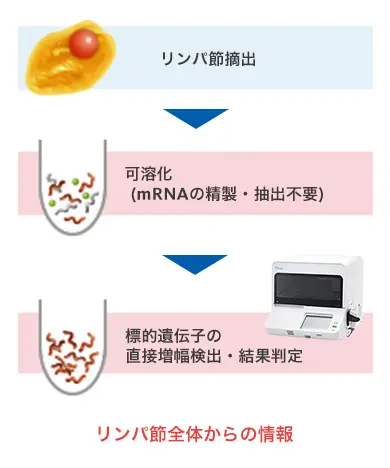
【OSNA™法(One-Step Nucleic Acid Amplification法)】
専用の装置と試薬で
がん細胞の遺伝子を増幅して測定
リンパ節全体を可溶化して検査するため、より正確な判定が可能です。検査開始から完了まで約30~40分と術中検査に使用できます。また、検査を自動化できるため、病理医の手技や熟練度による施設間差を解消することができます。
所要時間:約30~40分
メリット:
- リンパ節全体を検査するため、より高精度に判定が可能
- 短時間で検査結果を得られるため、手術中の検査が可能
- 検査を自動化できるため、測定方法の施設間差を解消
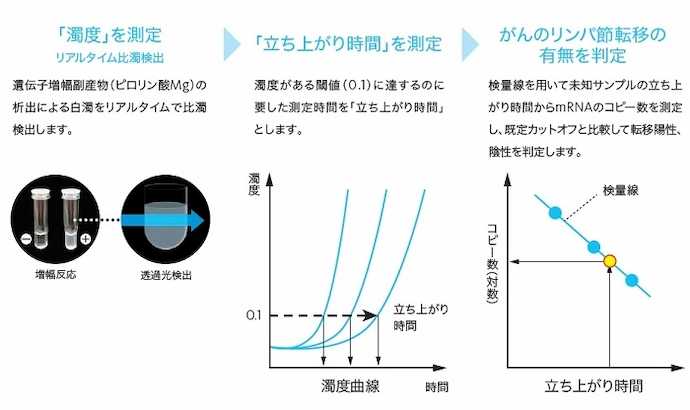
標的遺伝子の検出方法
リアルタイム濁度検出
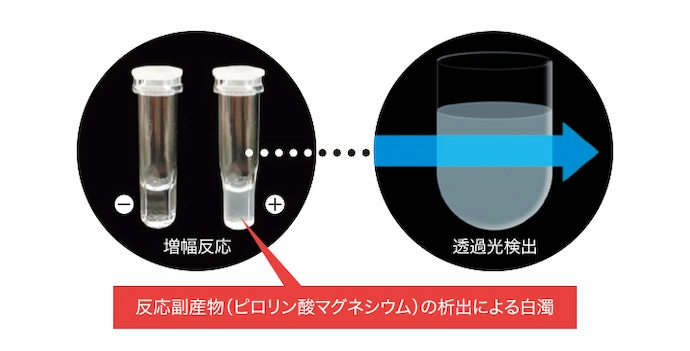
OSNA™法で遺伝子増幅法として採用しているRT-LAMP法*では、標的遺伝子の遺伝子増幅に伴い反応副産物としてピロリン酸マグネシウムが析出します。専用の解析装置は、この反応副産物の析出による濁度の変化をリアルタイムに検出しています。
- *RT-LAMP法
(Reverse Transcript Loop-Mediated Isothermal Amplification method)
当社はLAMP法の使用に関して栄研化学株式会社と2001年1月に実施権の許諾契約を締結しております。
mRNA濃度と立ち上がり時間との関係
リアルタイム検出している濁度がある閾値(0.1)に達した測定時間を「立ち上がり時間」としています。この「立ち上がり時間」はmRNA濃度(copies/μL)と相関関係があるため、予めmRNA濃度既知のキャリブレーターを用いて検量線を作成する事で、未知の測定サンプルの「立ち上がり時間」からmRNA濃度の定量が可能です。
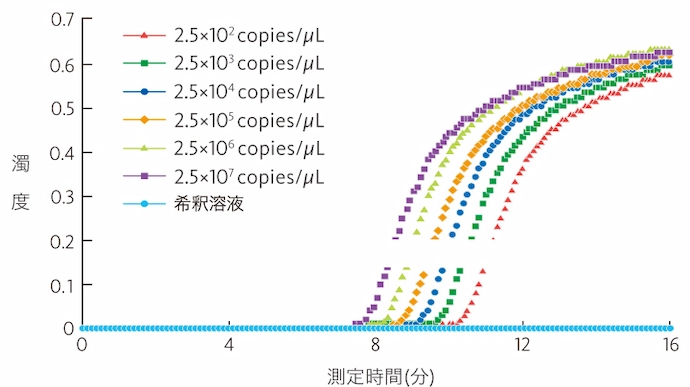
RT-LAMP法の増幅曲線
mRNA濃度(copies/μL)が高いほど立ち上がり時間が早い
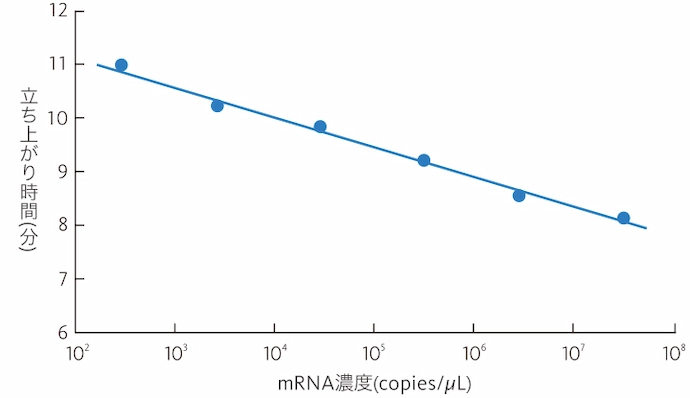
「立ち上がり時間」とmRNA濃度の関係
mRNA濃度(対数値)と「立ち上がり時間」は直線関係となり、これを検量線として測定サンプル中のmRNA濃度を算出します。
- ※実際には濃度既知の3点のキャリブレーターを用いて検量線を作成します。
遺伝子増幅検出装置 RD-200

OSNA™法専用の遺伝子増幅検出装置です。
測定サンプル、リノアンプ™CK19、消耗品をセットした後、遺伝子増幅・検出をすべて自動で行います。
| 処理能力※1 | 29分30秒以内/1バッチ(14サンプル+コントロール2種) |
|---|---|
| 消耗品架設数 | ピペットチップ:最大108本、検出セル:最大8個 |
| 表示項目 | Diagnostics Parameter項目: サイトケラチン19(CK19)mRNA定性判定(CK19 Q.) Service information項目: サイトケラチン19(CK19) mRNA定性判定(CK19 Q.) サイトケラチン19(CK19) mRNA半定量情報(CK19 SQ.) サイトケラチン19(CK19) mRNA濃度(CK19 C.) サイトケラチン19(CK19) mRNA立ち上がり時間(CK19) βアクチンmRNA濃度(Bactin C.)※2 βアクチンmRNA立ち上がり時間(Bactin)※2 |
| 反応に必要な試薬量 | プライマー溶液:20μL/テスト 酵素溶液:3μL/テスト |
| 反応に必要なサンプル量 | 2μL/テスト |
| データ出力 | 測定結果のバッチ印刷、CSVファイル出力、ホストコンピュータへの出力が可能 |
| 電源/消費電力 | 100~240V(50Hz/60Hz)/ 900VA以下 |
| 寸法 | (W)約600mm×(H)約610mm×(D)約780mm |
| 測定部重量 | 約90kg |
※2:リノアンプCK(LAC-A)に含まれるβアクチン試薬を使用した際に表示される項目
医療機器製造販売届出番号
28B1X10014000040
サイトケラチン19mRNAキット リノアンプ™CK19
摘出された乳癌、大腸癌、胃癌、非小細胞肺癌、子宮頸癌又は子宮体癌所属リンパ節のサイトケラチン19(CK19)mRNAの検出(乳癌、大腸癌、胃癌、非小細胞肺癌、子宮頸癌又は子宮体癌におけるリンパ節転移の診断補助)を目的とするOSNA™法専用の体外診断用医薬品です。 プライマー、酵素、キャリブレーター、およびコントロールを含みます。
| 品目コード | BX673729 |
|---|---|
| 使用目的 | 摘出された乳癌、大腸癌、胃癌、非小細胞肺癌、子宮頸癌又は子宮体癌所属リンパ節のCK19mRNAの検出(乳癌、大腸癌、胃癌、非小細胞肺癌、子宮頸癌又は子宮体癌におけるリンパ節転移の診断補助) |
| 貯蔵方法 | -25~-15℃ |
| 有効期間 | 12ヵ月 |
| 開封後の使用期間 | 2ヵ月 |
| 包装単位 | 120テスト用(LAC-701A) CK19プライマー溶液:1400μL×3本 酵素溶液:450μL×1本 CK19キャリブレーターレベル1:110μL×3本 CK19キャリブレーターレベル2:110μL×3本 CK19キャリブレーターレベル3:110μL×3本 CK19 陽性コントロール:110μL×3本 陰性コントロール: 110μL×3本 |
| 品目コード | BM386080 |
|---|---|
| 使用目的 | 摘出された乳癌、大腸癌、胃癌、非小細胞肺癌、子宮頸癌又は子宮体癌所属リンパ節のCK19mRNAの検出(乳癌、大腸癌、胃癌、非小細胞肺癌、子宮頸癌又は子宮体癌におけるリンパ節転移の診断補助) |
| 貯蔵方法 | -25~-15℃ |
| 有効期間 | 12ヵ月 |
| 開封後の使用期間 | 2ヵ月 |
| 包装単位 | 120テスト用(LAC-700A) CK19プライマー溶液:1400μL×2本 酵素溶液:450μL×1本 CK19キャリブレーター レベル1:110μL×2本 CK19キャリブレーター レベル2:110μL×2本 CK19キャリブレーター レベル3:110μL×2本 CK19 陽性コントロール:110μL×2本 βアクチンプライマー溶液:920μL×2本 βアクチン陽性コントロール:110μL×2本 βアクチンカットオフコントロール:110μL×2本 陰性コントロール: 110μL×2本 |
保険適用情報
乳がん、大腸がん、胃がん、非小細胞肺がん(保険点数:2400点)
医療機器製造販売届出番号
23000EZX00019000
遺伝子増幅検出装置 RD-100i

OSNA™法専用の遺伝子増幅検出装置です。
測定サンプル、リノアンプ™BC、消耗品をセットした後、遺伝子増幅・検出をすべて自動で行います。
- ※現在は販売を中止しております
| 処理能力 | 30分/1バッチ(4サンプル+コントロール2種) |
|---|---|
| 測定項目/演算項目 | 測定項目:mRNA定性判定値 演算項目:mRNA立ち上がり時間 mRNA濃度 |
| 所要試薬、サンプル量 | プライマー溶液:20μL/テスト、酵素溶液:3μL/テスト、サンプル:2μL/テスト |
| CSVファイル出力 | 測定結果リストをCSV形式のファイルとして出力可能 |
| 電源/消費電力 | 100~240V(50Hz/60Hz)/700VA以下(測定部) |
| 測定部寸法 | (W)約596mm×(H)約548mm×(D)約622mm |
| 測定部重量 | 約66kg |
医療機器製造販売届出番号
28B1X10014000032
サイトケラチン19mRNAキット リノアンプ™BC

摘出された乳がん、大腸がん、胃がん又は非小細胞肺がん所属リンパ節中のサイトケラチン19(CK19)mRNAの検出を目的とするOSNA™法専用の体外診断用医薬品です。 プライマー、酵素、キャリブレーター、およびコントロールを含みます。
| 使用目的 | 摘出された乳がん、大腸がん、胃がん又は非小細胞肺がんの所属リンパ節中のCK19mRNAの検出 (乳がん、大腸がん、胃がん又は非小細胞肺がんにおけるリンパ節転移診断の補助に用いる) |
|---|---|
| 保存方法及び有効期限 | 保存方法:-20℃ 有効期間:12ヵ月 |
| 開封後の使用期間 | 1ヵ月 |
| 包装単位 | CK19プライマー溶液:約720μL×8本 酵素溶液:約450μL×2本 CK19陽性コントロール:約110μL×4本 CK19陰性コントロール:約110μL×4本 キャリブレーターレベル1:約110μL×4本 キャリブレーターレベル2:約110μL×4本 キャリブレーターレベル3:約110μL×4本 |
保険適用情報
乳がん、大腸がん、胃がん、非小細胞肺がん(保険点数:2400点)
医療機器製造販売届出番号
22000AMX01627000
リンパ節前処理装置 RP-10

遺伝子増幅検出装置RD-100i、RD-200で測定するためのリンパ節ホモジナイズ工程において、自動で最大4個のリンパ節を同時に迅速かつ簡便・安全に破砕します。
特長
- 迅速性
最大4個のリンパ節を同時に破砕することでOSNA™法によるリンパ節転移検査の時間を短縮できます。(リンパ節4個の場合、約8%低減)
- 簡便性
リンパ節と可溶化試薬リノアーグを入れたホモジナイズ容器とディスポーザブルブレードをセットし、スタートボタンを押すだけでリンパ節を破砕します。
- 安全性
リンパ節の破砕・可溶化におけるオペレーターの手技のばらつきを低減します。また、リンパ節破砕時にオペレーターと周囲環境への飛沫拡散を抑えることができます。
| 処理能力 | 1分30秒/1パッチ(4検体) |
|---|---|
| 消耗品架設数 | ディスポーザブルブレード;最大4本、ホモジナイズ容量:最大4本 |
| 所要試薬量 | リノアーグ:4ml/検体 |
| 所要検体量 | リンパ節組織:25~600mg/検体 |
| 試薬と検体の保冷 | 検体ラックはクラッシュアイスによる冷却が可能 |
| 電源/消費電力 | 100~240V(50Hz/60Hz)/ 500VA 以下 |
| 寸法 | (W)391mm×(H)500mm×(D)267mm |
| 重量 | 約23kg |
医療機器製造販売届出番号
28B1X10014000037
リノアーグ™
OSNA™法専用の検体可溶化試薬です。
細胞を可溶化する際に用い、可溶化液中でのmRNAを安定的に保持します。
| 使用目的 | 遺伝子増幅検出装置RD-100i、RD-200用測定試料の調製 |
|---|---|
| 貯蔵方法 | 2℃~8℃ |
| 有効期限 | 12ヵ月 |
| 開封後の使用期間 | 2ヵ月 |
| 包装単位 | 110ml×1本(24リンパ節分) |
リノプレップブレードセット/リノプレップアダプターN

OSNA™法の前処理用ディスポーザブルブレードです。
ワンタッチでブレードを装着することができ、使用後の洗浄・滅菌が不要です。
| 使用目的 | リンパ節をホモジナイズするためのブレード (ディスポーザブルタイプ) |
|---|---|
| 包装単位 | リノプレップブレードセット:ブレード 12本 ホモジナイズ容器 12本 リノプレップ アダプターN:1個 |
ピペットチップ

| 梱包単位 | 36本/ラック×10ラック/箱 |
|---|---|
| 使用量 | 1テストあたり3本使用 |
検出セル

| 梱包単位 | 2穴/セル×50個/箱 |
|---|---|
| 使用量 | 1テストあたり1穴使用 |
RD サンプルバイアル

| 品目コード | BP675300 |
|---|---|
| 梱包単位 | 100本 |
| 使用量 | 1リンパ節あたり1本(RD-200の場合) |
その他必要な備品・消耗品
- ※メーカー指定品およびメーカー推奨品がございます。詳しくは弊社までお問い合わせください。
| その他必要な備品・消耗品 | 用途 |
|---|---|
| ハンディーホモジナイザー | リンパ節の可溶化 |
| ホモジナイザー用シャフト | リンパ節の可溶化 (シスメックス製品”リノプレップブレードセット”を使用する場合は必要ありません。) |
| 遠心機 (10,000G対応、 1.5mLチューブ搭載可) |
リンパ節可溶化液の遠心分離 |
| 卓上遠心機 | 試薬・サンプルの気泡除去 (上記遠心機に同様の機能が含まれている場合は必要ありません。) |
| ボルテックスミキサー | 試薬・サンプルの撹拌 |
| 50mLチューブ | リンパ節を入れて可溶化 (シスメックス製品”リノプレップブレードセット”を使用する場合は必要ありません。) |
| 1.5mLチューブ | サンプル調製容器 |
| 0.5mLスクリューキャップ付マイクロチューブ | サンプル容器 |
| マイクロピペット (推奨:20μL、180μL、1mL対応の3種類) |
サンプル分注 |
| ピペットチップ (マイクロピペット各種に対応する) | サンプル分注(フィルター付きを推奨) |
| 超音波洗浄器 | ホモジナイザー用シャフトの洗浄 (シスメックス製品”リノプレップブレードセット”を使用する場合は必要ありません。) |
| オートクレーブ | ホモジナイザー用シャフトの減菌 (シスメックス製品”リノプレップブレードセット”を使用する場合は必要ありません。) |
| メディカルフリーザー(-20℃) | リノアンプ™CK19またはリノアンプ™BCの保管 |
OSNA™の臨床性能を評価するため、病理組織検査との比較による臨床性能試験を行いました。
乳がんリンパ節転移検査に関するデータ
OSNA™が転移陰性リンパ節を陽性と判断(偽陽性)しないことを示すため、病理組織検査との陰性一致率(特異度)を評価しました。
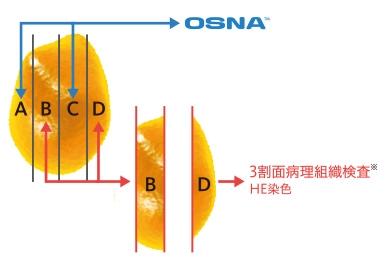
- ※ブロックB及びDから200μm間隔で連続した1対の標本(厚さ5μm)を作製し、一方をHE染色、他方を抗CK19抗体による免疫染色を行い、転移有無の判定を行いました。
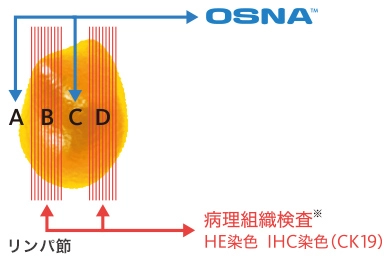
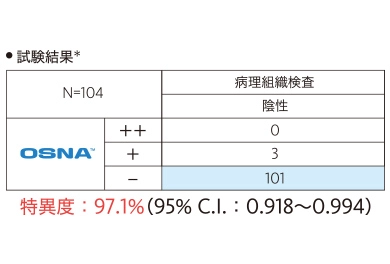
この試験において、OSNA™は転移陰性リンパ節に対して高い特異度を示すことが確認されました。
出典:Clinical Cancer Research, 2009 15:2879-2884
術後に行われている、永久標本3割面を用いる病理組織検査と、OSNA™の結果を比較して、判定結果の同等性(一致率)を評価しました。
- ※ブロックB及びDの割面から1対の標本(厚さ5μm)を作製し、一方をHE染色、他方を抗CK19抗体による免疫染色を行い、転移有無の判定を行いました。
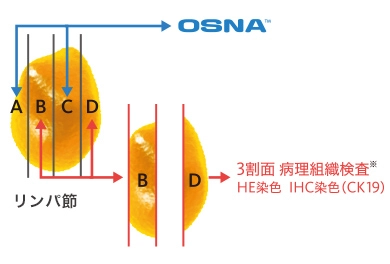
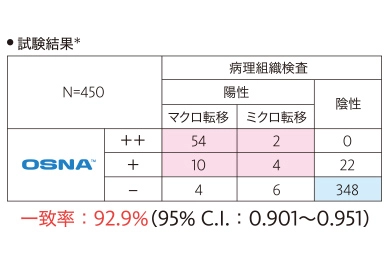
この試験において、病理組織検査とOSNA™の判定結果は高い一致率を示しました。
出典:Clinical Cancer Research, 2009 15:2879-2884
OSNA™の術前薬物療法受療症例における臨床性能を評価するため、病理組織検査との比較による臨床研究を行いました。
永久標本を用いた2mm間隔病理組織検査と、OSNA™の結果を比較して、判定結果の同等性(一致率)を評価しました。
- ※ブロックB及びDの割面から1対の標本を作製し、一方をHE染色、他方を抗CK19抗体による免疫染色を行い、転移有無の判定を行いました。
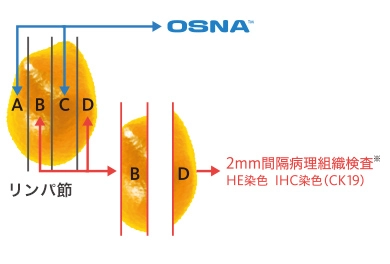
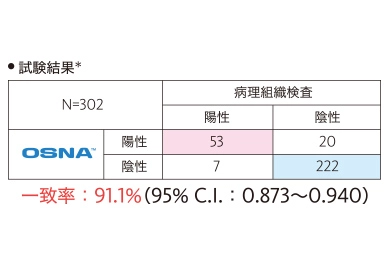
この研究において、病理組織検査とOSNA™の判定結果は高い一致率を示しました。
- ※術前薬物療法として主にアンスラサイクリン、タキサン、シクロフォスファミド、5-FUが投与された症例における成績です。その他の薬剤投与例については十分な検討ができておりません。
大腸がんリンパ節転移検査に関するデータ
病理組織検査により陰性と判定されたリンパ節をOSNA™により測定し、陰性一致率(特異度)を評価しました。
- ※ブロックB及びDから100μm間隔で連続した1対の標本(厚さ5μm)を作製し、一方をHE染色、他方を抗CK19抗体による免疫染色を行い、転移有無の判定を行いました。
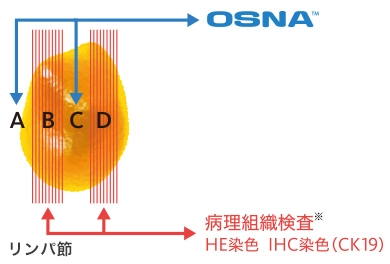
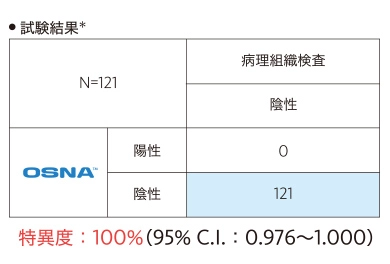
この試験において、OSNA™は転移陰性リンパ節に対して高い特異度を示すことが確認されました。
2mm間隔病理組織検査と、OSNA™の結果を比較して、判定結果の同等性(一致率)を評価しました。
- ※ブロックB及びDの割面からHE染色標本(厚さ5μm)を作製し、転移有無の判定を行いました。
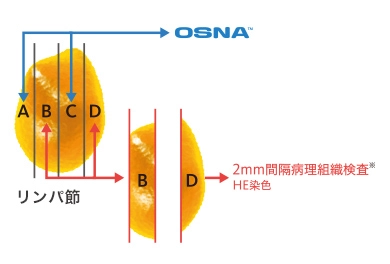
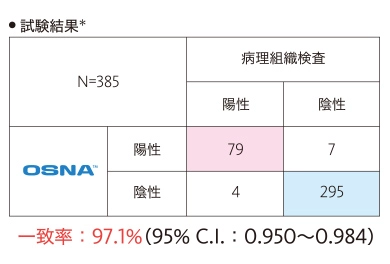
この試験において、病理組織検査とOSNA™の判定結果は高い一致率を示しました。
胃がんリンパ節転移検査に関するデータ
61症例394リンパ節を用いて2mm間隔病理組織検査と、OSNA™の結果を比較して、判定結果の同等性(一致率)を評価しました。
- ※ブロックB及びDの割面からHE染色標本(厚さ5μm)を作製し、転移有無の判定を行いました。
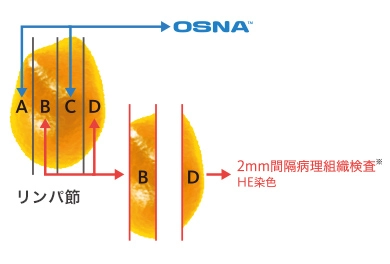
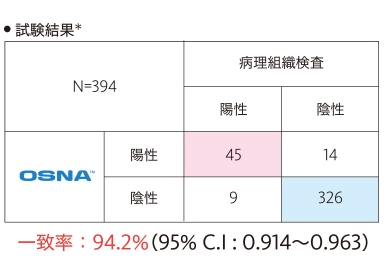
この試験において、病理組織検査とOSNA™の判定結果は高い一致率を示しました。
上記61症例のうち、病理組織学的転移陰性症例のリンパ節について層別解析を行い、特異度(陰性一致率)を評価しました。
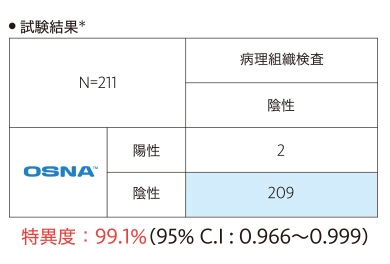
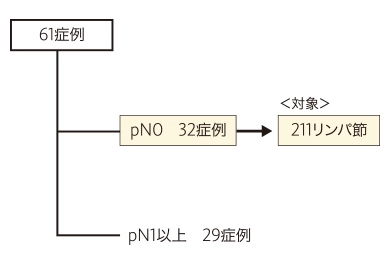
この試験において、OSNA™は転移陰性リンパ節に対して高い特異度を示すことが確認されました。
非小細胞肺がんリンパ節転移検査に関するデータ
111症例410リンパ節を用いて3割面病理組織検査とOSNA™法との一致率を評価しました。
- ※ブロックB及びDの割面から標本(厚さ5μm)を作製し、HE染色を行い、転移有無の判定を行いました。
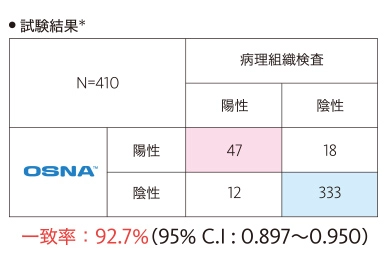
この試験において、病理組織検査とOSNA™の判定結果は高い一致率を示しました。
出典:リノアンプ®BCの添付文書より引用
上記111症例のうち、病理組織学的転移陰性例63症例の227リンパ節について層別解析を行い、陰性一致率(特異度)を評価しました。
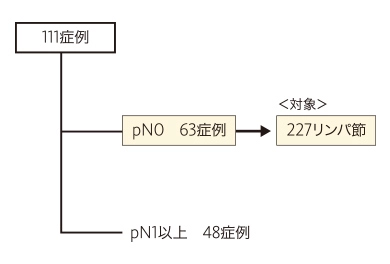
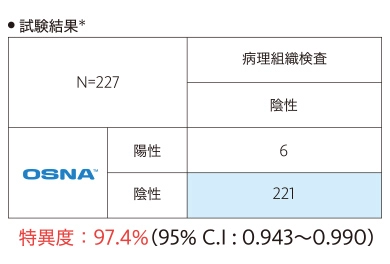
この試験において、OSNA™は転移陰性リンパ節に対して高い特異度を示すことが確認されました。
出典:リノアンプ®BCの添付文書より引用
非小細胞肺がんにおけるOSNA法導入による臨床上の有用性
- ※クリックして拡大
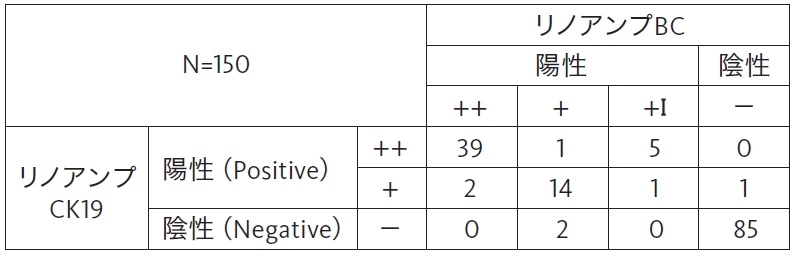
リノアンプBCとリノアンプCK19との相関性
乳癌所属リンパ節における「リノアンプBC」 及びリノアンプCK19の判定結果の一致率は98.0%(95%信頼区間94.3~99.3%)でした。

参考結果: (++), +i判定を含めた判定
大腸癌所属リンパ節における一致率は96.0%(95%信頼区間91.5~98.1%)でした。
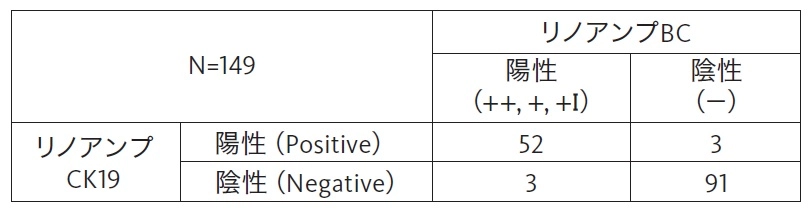
胃癌所属リンパ節における一致率99.3 %でした。

非小細胞肺癌所属リンパ節における一致率は96.2%(95%信頼区間92.0~98.3%)でした。

製品カタログ
- ※画像をクリックするとカタログをダウンロードしていただけます。
添付文書
独立行政法人医薬品医療機器総合機構(PMDA)新規ウィンドウを開きますのホームページにてご確認ください。
学術資料
基礎検討
関連文献
乳がん
- Kenzo Shimazu. et al. : One-step Nucleic Acid Amplification Can Identify Sentinel Node-negative Breast Cancer Patients With Excellent Prognosis : ANTICANCER RESEARCH 39 : 1447-1454 (2019)
- Kenzo Shimazu. et al. : Performance of a new system using a one step nucleic acid amplifcation assay for detecting lymph node metastases in breast cancer : Medical Oncology 2019 36:54
- Kenzo Shimazu. et al. : Intraoperative Nomograms, Based on One-Step Nucleic Acid Amplification, for Prediction of Non-sentinel Node Metastasis and Four or More Axillary Node Metastases in Breast Cancer Patients with Sentinel Node Metastasis : Ann Surg Oncol (2018) 25:2603–2611
- Tomo Osako. et al. : A new molecular-based lymph node staging classification determines the prognosis of breast cancer patients : British Jounal of Cancer 2017
- Vicente Peg . et al. : Role of total tumour load of sentinel lymph node on survival in early breast cancer patients : The Breast 33 (2017) 8e13
- Tsujimoto M. et al. : One-step Nucleic Acid Amplification for Intraoperative Detection of Lymph Node Metastasis in Breast Cancer Patients : Clinical Cancer Research, 13: 4807-4816, 2007
大腸がん
- Yamamoto H.Micrometastasis in lymph nodes of colorectal cancer.Ann Gastroenterol Surg.2022 May 26;6(4):466-473.
- Yukiharu Hiyoshi et al. : The advantage of one-step nucleic acid amplification for the diagnosis of lymph node metastasis in colorectal cancer patients. : Annals of Gastroenterological Surgery. 2020
- Michio Itabashi et al. : Lymph Node Positivity in One-Step Nucleic Acid Amplification is a Prognostic Factor for Postoperative Cancer Recurrence in Patients with Stage II Colorectal Cancer: A Prospective, Multicenter Study. : Ann Surg Oncol. 2019
- Sherley Diaz‑Mercedes et al. : Budget Impact Analysis of Molecular Lymph Node Staging Versus Conventional Histopathology Staging in Colorectal Carcinoma : Appl Health Econ Health Policy. 2019
- Maria José BRITO et al. : Molecular Staging of Patients with Colon Cancer. The C-Closer-II Study: A Multicentre Study in Portugal : Acta Med Port. 2018
- Miyake Y et al. : Inspection of Perirectal Lymph Nodes by One-Step Nucleic Acid Amplification Predicts Lateral Lymph Node Metastasis in Advanced Rectal Cancer. : Ann Surg Oncol. 2017
- Wild JB et al. : Is it time for one-step nucleic acid amplification (OSNA) in colorectal cancer? A systematic review and meta-analysis. : Tech Coloproctol. 2017
胃がん
- Ayako Shimada et al. : Utility of the one-step nucleic acid amplification assay in sentinel node mapping for early gastric cancer patients : Gastric Cancer. 2019
- Shoji Y et al. : Prospective feasibility study for single-tracer sentinel node mapping by ICG (indocyanine green) fluorescence and OSNA (one-step nucleic acid amplification) assay in laparoscopic gastric cancer surgery : Gastric Cancer. 2019
- Kumagai K, et al. : Multicenter study evaluating the clinical performance of the OSNA® assay for the molecular detection of lymph node metastases in gastric cancer patients. : Gastric Cancer. 2013
- Miyashiro I et al. : What Is the Problem in Clinical Application of Sentinel Node Concept to Gastric Cancer Surgery? : J Gastric Cancer. 2012
- Yaguchi Y, et al. : One-Step Nucleic Acid Amplification (OSNA®) for the Application of Sentinel Node Concept in Gastric Cancer : Annals of Surgical Oncology. 2011
非小細胞肺がん
- Naoko Ose.et al.Detection of lymph node metastasis in non-small cell lung cancer using the new system of one-step nucleic acid amplification assay.PLoS One. 2022 Mar 21;17(3):e0265603.
- Escalante Pérez M, et al. : Detection of lymph node metastasis in lung cancer patients using a one-step nucleic acid amplification assay: a single-centre prospective study. : J Transl Med. 2019
- Zhou M, et al. : The diagnostic value of one step nucleic acid amplification (OSNA) in differentiating lymph node metastasis of tumors: A systematic review and meta-analysis. : Int J Surg. 2018
- Vodička J, et al. : Can the One-Step Nucleic Acid Amplification method of lymph nodes examination make the staging of pulmonary tumours more precise? : Rozhl Chir. 2018
- Vodička J, et al. : A more sensitive detection of micrometastases of NSCLC in lymph nodes using the one-step nucleic acid amplification (OSNA) method. : J Surg Oncol. 2017
- Nakagawa K, et al. : The novel one-step nucleic acid amplification (OSNA) assay for the diagnosis of lymph node metastasis in patients with non-small cell lung cancer (NSCLC): Results of a multicenter prospective study. : Lung Cancer. 2016
婦人科がん
- Shinichi Togami. et al.Evaluation of the one-step nucleic acid amplification assay for detecting lymph node metastasis in patients with cervical and endometrial cancer: A multicenter prospective study. Gynecologic Oncology 170 (2023) 70–76
- Shinichi Togami. et al.One-step nucleic acid amplification (OSNA) assay for detecting lymph node metastasis in cervical and endometrial cancer: a preliminary study.J Gynecol Oncol. 2022 Mar;33(2):e11.
- María Dolores Diestro et al.Cancers (Basel) et al.One-Step Nucleic Acid Amplification (OSNA) of Sentinel Lymph Node in Early-Stage Endometrial Cancer: Spanish Multicenter Study (ENDO-OSNA).2021 Sep; 13(17): 4465
- T nagai et al.A new diagnostic method for rapid detection of lymph node metastases using a one-step nucleic acid amplification (OSNA) assay in endometrial cancer.Ann Surg Oncol. 2015 Mar;22(3):980-6.
お問い合わせ先
製品に関するご質問・ご相談は、下記よりお気軽にご連絡ください。